آغاز اولین کارآزمایی بالینی CRISPR در سال 2018
محققان شرکتی دارویی برای اولین بار تصمیم گرفتند در سال ۲۰۱۸ از تکنیک ویرایش ژن کریسپر در درمان بالینی انسان استفاده کننند. آنها با دریافت اجازهٔ رسمی از مجامع قانونی اروپا توانستند مجوز آزمایش درمان کمخونی داسیشکل و تالاسمی بتا را توسط CTX001 که یک درمان کریسپر است، بهدست آورند.
داستانهای ژول ورن و ایزاک آسیموف بعد از سالها تحقق یافتند و همگان مبهوت نبوغ نویسندگان این داستانها شدند؛ اما کریسپر رویایی بود که هیچکس گمان نمیکرد با چنین سرعتی به این جایگاه خارقالعاده در علم ژنتیک و درمان بیماریها دست یابد.
محققان شرکتی دارویی برای اولین بار تصمیم گرفتند در سال ۲۰۱۸ از تکنیک ویرایش ژن کریسپر در درمان بالینی انسان استفاده کننند. آنها با دریافت اجازهٔ رسمی از مجامع قانونی اروپا توانستند مجوز آزمایش درمان کمخونی داسیشکل و تالاسمی بتا را توسط CTX001 که یک درمان کریسپر است، بهدست آورند.
مدیرعامل این شرکت، سامارت کولکارنی، در مصاحبهای چنین میگوید: به گمان من این رویداد اتفاقی خاص برای ما و این مرحله از علم است. تا همین سه سال پیش هم تصور میشد که درمان با کریسپر تنها داستانی علمی-تخیلی است، اما هماکنون حقیقت چیز دیگری است.
CRISPER نوعی تکنیک ویرایش ژنها است که از سیستم دفاعی باکتریها بهدست آمدهاست. به عبارت دیگر و کلیتر، یک سیستم با قابلیت برنامهریزی است که بخش خاصی از DNA را مورد هدف و ویرایش قرار میدهد و میتواند به عنوان یک ابزار تشخیصی نیز به کار رود.
مفهوم ویرایش ژن در ابتدا بخشی از یک کابوس علمی-تخیلی به نظر میرسید که در آن ما در حال انجام کنترلی ناپسند از منظر اخلاق زیستشناسی هستیم؛ اما همانطور که فناوری پیشرفت کردهاست و پتانسیل باورنکردنی ویرایش ژن بیشتر مورد بررسی قرار گرفتهاست، CRISPR نیز بیشتر به عنوان یک ابزار نوآورانه که توانایی نجات جان انسانها را دارد، محسوب میشود.
این موضوع در این کارآزمایی بالینی مشهود است؛ چرا که هر دو بیمار مبتلا به بیماری سلول داسیشکل یا بتا تالاسمی دارای جهشهای ژنتیکی خاصی هستند که به طور ناگهانی بر بخشی از هموگلوبین تأثیر میگذارد که به توانایی سلولهای قرمز در انتقال اکسیژن به بدن مرتبط است. جهشها میتوانند سبب علایمی نظیر خستگی، زردی، درد شدید و به طور بالقوه مرگ شوند. در درمانی که در این آزمایشها بررسی میشود، CTX001، با برش یک ژن که باعث تولید هموگلوبین جنینی میشود، عمل میکند. این شکل جنینی از هموگلوبین هنگامی که نوزاد شروع به تشکیل فرم بالغ میکند خاموش میشود، اما از آنجا که شکل بالغ در بیماران مبتلا به بیماری سلول داسیشکل یا بتا تالاسمی جهش یافتهاست، تبدیل هموگلوبین به حالت جنینی باعث میشود سلولهای قرمز خون به طور مؤثر دوباره به حمل تاثیرگذار اکسیژن بپردازد.
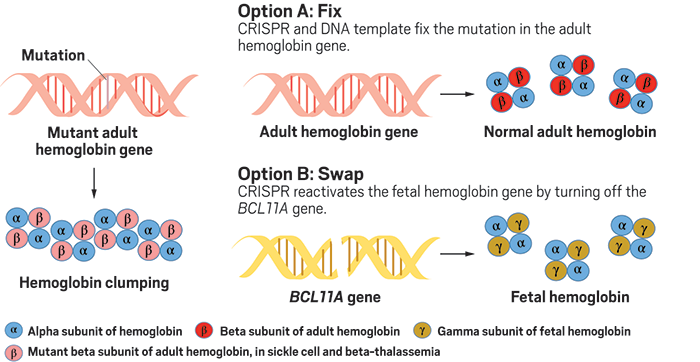
با توجه به اطلاعات جمعآوریشده از طریق آزمایشهای سلولی و حیوانی، که توسط این شرکت در جلسهٔ انجمن هماتولوژی آمریکا در آتلانتا ارائه شدهاست، CTX001 در ویرایش این ژن بسیار کارآمد است و تا کنون نشانههایی از تأثیرات بر روی ژنهای دیگر را نشان ندادهاست.
اگر این کارآزمایی بالینی موفقیتآمیز باشد یا حداقل عوارض مضر را ایجاد نکند، میتواند آیندهای طولانی از درمانهای نوآورانه و فراتر از مرزها را با CRISPR ایجاد کند. از مقاومت آنتیبیوتیک تا تغییر بیماری و ریشهکنسازی آن، ویرایش ژن میتواند یک اصل جدید در پزشکی آینده باشد.
لینک مطلب: C & EN
پایان مطلب / ادمین


ارسال به دوستان