ژندرمانی انقلابی، مسیر درمان سرطان خون مقاوم را تغییر داد.
پژوهشگران بریتانیایی با توسعه یک روش پیشرفته ژندرمانی موفق شدهاند در برخی بیماران مبتلا به نوعی نادر و بسیار تهاجمی از سرطان خون، بیماریای که پیشتر غیرقابل درمان تلقی میشد، بهبودی پایدار ایجاد کنند.
پژوهشگران بریتانیایی با توسعه یک روش پیشرفته ژندرمانی موفق شدهاند در برخی بیماران مبتلا به نوعی نادر و بسیار تهاجمی از سرطان خون، بیماریای که پیشتر غیرقابل درمان تلقی میشد، بهبودی پایدار ایجاد کنند. نتایج این دستاورد مهم که در دسامبر ۲۰۲۵، در مجله معتبر New England Journal of Medicine منتشر شده، امید تازهای برای بیماران مبتلا به سرطانهای خونی مقاوم به درمان فراهم کرده است.
این درمان نوین بر پایه ویرایش بسیار دقیق DNA در سلولهای سفید خون بنا شده و سلولهای ایمنی را به یک داروی زنده علیه سرطان تبدیل میکند. در این روش، سلولهای T که در حالت طبیعی وظیفه دفاع از بدن را بر عهده دارند، بهگونهای مهندسی میشوند که بهطور هدفمند سلولهای سرطانی را شناسایی و نابود کنند.
در این کارآزمایی بالینی، هشت کودک و دو بزرگسال مبتلا به لوسمی لنفوبلاستیک حاد سلول T (T-ALL)، که به شیمیدرمانی و حتی پیوند مغز استخوان پاسخ نداده بودند، تحت درمان قرار گرفتند. این بیماران پیش از ورود به مطالعه، گزینه درمانی مؤثری نداشتند و در برخی موارد تنها مراقبتهای تسکینی برای آنها مطرح بود. با این حال، نتایج نشان داد که حدود ۶۴ درصد بیماران وارد بهبودی عمیق و پایدار شده و تا سه سال پس از درمان بدون نشانهای از بیماری باقی ماندهاند.
ویرایش هدفمند DNA؛ قلب فناوری BE-CAR7
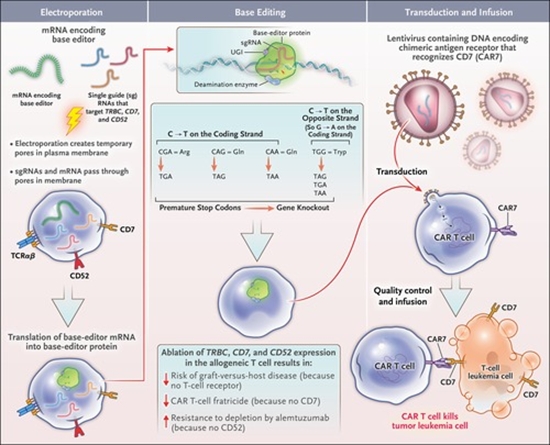
پژوهشگران دانشگاه کالج لندن (UCL) و بیمارستان Great Ormond Street از فناوریای موسوم به «Base Editing» استفاده کردند؛ روشی که امکان تغییر دقیق تنها یک «حرف» از کد ژنتیکی را فراهم میکند. همانگونه که تغییر یک حرف در یک کلمه میتواند معنای جمله را عوض کند، این ویرایشهای کوچک ژنتیکی نیز میتوانند عملکرد سلول را بهطور اساسی تغییر دهند.در این درمان، سلولهای T اهداکننده طی چند مرحله ویرایش ژنتیکی شدند: ابتدا توانایی آنها برای حمله به بدن بیمار غیرفعال شد، سپس نشانگر سطحی CD7 که روی تمام سلولهای T وجود دارد حذف شد تا سلولهای درمانی به یکدیگر حمله نکنند. در مرحله بعد، این سلولها در برابر برخی داروهای شیمیدرمانی مقاوم شدند و در نهایت بهگونهای برنامهریزی شدند که هر سلول دارای نشانگر CD7 را نابود کنند.در نتیجه، سلولهای اصلاحشده پس از تزریق، تمام سلولهای T بیمار – چه سرطانی و چه سالم – را از بین میبرند. در صورت پاکسازی کامل سرطان طی چهار هفته، بیماران میتوانند تحت پیوند مغز استخوان قرار گیرند تا سیستم ایمنی سالمی برای آنها بازسازی شود.
نتایج بالینی و تجربه بیمارانیکی از نخستین دریافتکنندگان این درمان، آلیسا تپلی، نوجوانی ۱۶ ساله بود که در سال ۲۰۲۲ اولین بیمار جهان برای دریافت این روش محسوب میشد. او که پیشتر امید چندانی به بقا نداشت، اکنون بدون نشانهای از سرطان زندگی میکند، به مدرسه بازگشته و حتی برنامه دارد در آینده وارد حوزه پژوهش سرطانهای خونی شود.
پزشکان شرکتکننده در این مطالعه تأکید میکنند که اگرچه این درمان بسیار پیچیده و سنگین است و خطراتی مانند عفونت در دوره حذف سیستم ایمنی را به همراه دارد، اما برای بیمارانی که تمامی درمانهای موجود در آنها شکست خورده بود، یک فرصت واقعی برای زندگی ایجاد کرده است.
به گفته متخصصان، هرچند این مطالعه در مرحله اولیه قرار دارد و نیازمند بررسیهای گستردهتر است، اما نتایج بهدستآمده نشاندهنده جهش مهمی در درمانهای ژنتیکی و سلولی بوده و میتواند مسیر آینده درمان سرطانهای خونی مقاوم را بهطور اساسی تغییر دهد.
نتایج بالینی و تجربه بیمارانیکی از نخستین دریافتکنندگان این درمان، آلیسا تپلی، نوجوانی ۱۶ ساله بود که در سال ۲۰۲۲ اولین بیمار جهان برای دریافت این روش محسوب میشد. او که پیشتر امید چندانی به بقا نداشت، اکنون بدون نشانهای از سرطان زندگی میکند، به مدرسه بازگشته و حتی برنامه دارد در آینده وارد حوزه پژوهش سرطانهای خونی شود.
پزشکان شرکتکننده در این مطالعه تأکید میکنند که اگرچه این درمان بسیار پیچیده و سنگین است و خطراتی مانند عفونت در دوره حذف سیستم ایمنی را به همراه دارد، اما برای بیمارانی که تمامی درمانهای موجود در آنها شکست خورده بود، یک فرصت واقعی برای زندگی ایجاد کرده است.
به گفته متخصصان، هرچند این مطالعه در مرحله اولیه قرار دارد و نیازمند بررسیهای گستردهتر است، اما نتایج بهدستآمده نشاندهنده جهش مهمی در درمانهای ژنتیکی و سلولی بوده و میتواند مسیر آینده درمان سرطانهای خونی مقاوم را بهطور اساسی تغییر دهد.
جهت کسب اطلاعات بیشتر به لینک مقاله مربوطه مراجعه فرمائید:


نظر دهید